Salze Chemie Klasse 9
Chemie Kl. 9, Realschule, Bayern 32 KB Sauerstoff, Redoxreaktionen (Luft), Salzsäure, Reaktion mit Metall oder Lauge Redoxreaktionen als Reaktion mit Sauerstoff und als Elektronenübertragung, edle und unedle Metalle, Eigenschaften und Aufbau von Säuren, pH-Wert Chemie Kl.
Salze chemie klasse 9 gymnasium
Salze chemie klasse 9.3
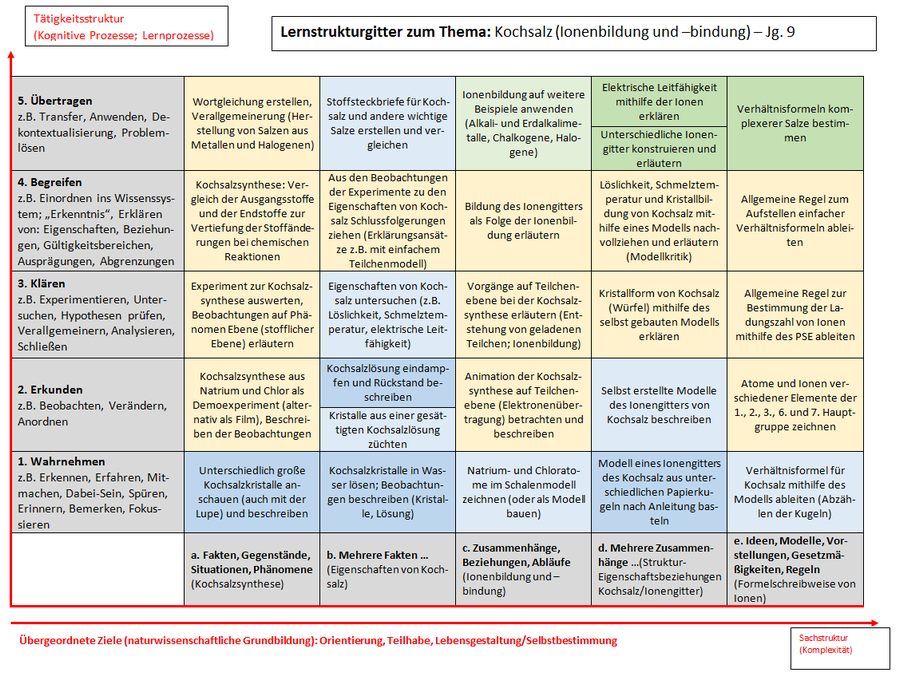
Sie bilden gemeinsam ein sog. Ionengitter. 3. Eigenschaften von Salzen harte Feststoffe sehr hoher Schmelzpunkt spröde, d. h. brechen bei Krafteinwirkung auseinander → Verschiebung von Gitter-Ebenen führt zu Abstoßungskräften, wenn gleichnamige Ladungen aufeinander treffen Elektrische Leitfähigkeit nicht im Feststoff, aber in der Schmelze → freie Beweglichkeit der Ionen in der Flüssigkeit⇒ Ladungsfluss 4. Elektrolyse von Salzen B am + Pol: rotbraune Schlieren am - Pol: grauer Überzug E am + Pol: elementares Iod am - Pol: elementares Zink Wanderung der Ionen zu dem entgegengesetzten Elektroden → "Entladung" Elektrodenreaktionen: Kathode (- Pol): 2e - + Zn 2+ → Zn Anode (+ Pol): 2I - → I 2 + 2e - Gesamtvorgang: Zn 2+ + 2I - → Zu + I 2 5. Molekülionen (Zusammengesetze Ionen) (= Ionen, die aus mindestens zwei verschiedenen Elementen bestehen, tragen eine Gesamtladung) Beispiel: N0 3 - Nitrat-Ion (Anion) NH 4 + Ammonium-Ion (Kation) Ca 3 (PO 4) 2 Kalziumphosphat KMnO 4 Kaliumpermanganat 6. Salzbildung Metall → Metallion (positiv geladen: Kation) M → M + + e - z. Na → Na + + e - Nichtmetall → Nichtmetallion (negativ geladen: Anion) e - + X → X - 2 e - + Cl 2 → 2 Cl - Kristallbildung von Salzen Was hält die Bestandteile eines Salzes zusammen?
Salze chemie klasse 9 mois
- Schleswig-Holstein | Oldtimerzentrale
- Salze chemie klasse 9
- Süd Apotheke in Coburg - Bayern - StreetDir.com
- Salze chemie klasse 9.0
- 20 to Shape - Bodyweight only: Fit ohne Geräte (Mängelexemplar), Ralf Ohrmann
- Quad händler bayern
- Profoto vs einstein
- Salze - Chemie in Alltag und Technik einfach erklärt!